É possível curar um coração partido com células?
Autores
Ana Spasojevic, Emilio I. Alarcon, Erik J. Suuronen, Marc Ruel
Jovens revisores

Resumo
Os cardiomiócitos são as células dos músculos que fazem o coração bater, bombeiam oxigênio e levam o sangue rico em nutrientes para todas as partes do corpo. Durante um ataque cardíaco, o suprimento de sangue para o coração é interrompido. Os cardiomiócitos então morrem e são substituídos por tecido cicatricial que já não consegue se contrair. Células-tronco são células-mestre que crescem e se dividem rapidamente e podem ser ideais para reparar órgãos e tecidos porque se transformam em vários tipos diferentes de células, inclusive cardiomiócitos. Entre outras terapias médicas, as células-tronco foram usadas para desenvolver o remendo cardíaco, uma espécie de “band-aid” que pode regenerar músculos cardíacos danificados. Neste artigo, discutiremos as vantagens e limitações do uso de células-tronco para o reparo de um “coração partido”.
Como o coração funciona?
Toda célula do corpo precisa de oxigênio e nutrientes para sobreviver. O sangue é o serviço de entrega do corpo, levando para as células os materiais de que elas precisam. O coração é a bomba que impele o sangue pelo corpo, quer estejamos dormindo, comendo, andando de bicicleta ou jogando videogame. O coração está sempre trabalhando, batendo cerca de 100 mil vezes por dia [1]. Ele tem quatro câmaras principais, que são como estações para o sangue (Figura 1).
O sangue pobre em oxigênio, voltando ao coração de sua longa jornada pelo corpo, “deságua” no átrio direito e em seguida flui para o ventrículo direito. Quando o coração se contrai, o ventrículo direito bombeia o sangue para os pulmões, onde ele se reabastece de oxigênio do ar inalado. Esse sangue agora rico em oxigênio volta ao coração, indo para o átrio esquerdo e depois para o ventrículo esquerdo. Finalmente, o ventrículo esquerdo se contrai de novo, bombeando o sangue rico em oxigênio para todas as células e órgãos do corpo. Quatro válvulas cardíacas controlam o fluxo sanguíneo entre cada uma das câmaras. As válvulas se abrem e fecham quando o sangue passa de uma câmara para outra, impedindo que ele reflua. Essas válvulas podem ser vistas como os “guardas de trânsito” do coração: garantem que o sangue flua apenas em uma direção pelas ruas “de mão única” do órgão.
Como é possível que seu coração bata sem você sequer ter consciência disso? Acontece que o coração possui seu próprio cerebrozinho, chamado nódulo sinoatrial (NS). O nódulo NS controla a atividade de seu coração independentemente do cérebro, enviando sinais elétricos que monitoram a contração muscular sincronizada. Além disso, cada câmara do coração possui mecanismos que assumem a função respiratória caso o nódulo NS falhe.
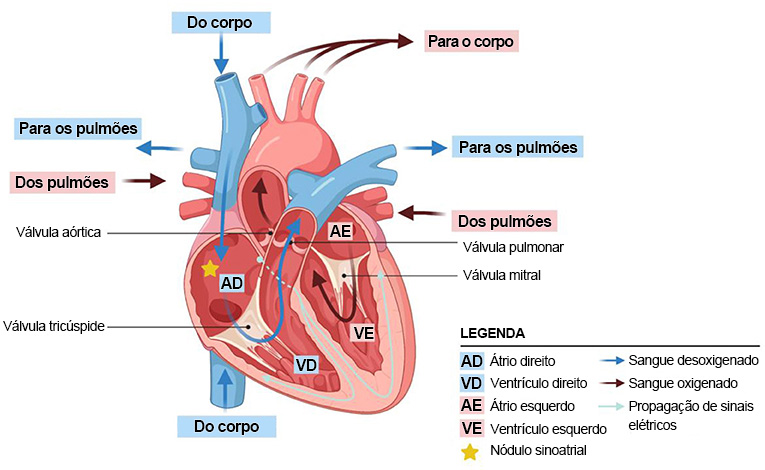
O coração mantém uma circulação de sangue constante pelo corpo. O sangue com pouco oxigênio vai para o coração a partir do corpo, flui pelo átrio direito e ventrículo direito, e é bombeado para os pulmões, onde se oxigena. O sangue oxigenado volta para o coração pelo átrio esquerdo, flui para o ventrículo esquerdo e é bombeado de volta para o corpo. Cada batimento cardíaco é acionado por sinais elétricos que coordenam a contração de cardiomiócitos.
As células musculares do coração são chamadas de cardiomiócitos. Em média, o coração humano contém de 2 a 3 bilhões de cardiomiócitos [2]. Como todas essas células sabem quando se contrair para produzir um único e forte batimento cardíaco? As membranas celulares se ligam em junções especiais que mantêm as células unidas e permitem a passagem de moléculas mensageiras que instruem as células a bater. Desse modo, os cardiomiócitos se comportam como uma única unidade funcional. Eles trabalham em equipe para bombear sangue pelo corpo.
Quando o coração falha: história de um ataque cardíaco
Assim como as células de outros órgãos do corpo, os cardiomiócitos precisam de oxigênio e nutrientes para funcionar. Desse modo, o coração tem sua própria rede de vasos sanguíneos – artérias e veias que envolvem o coração inteiro. O coração pode parecer um órgão perfeito, mas tem suas falhas. Os ataques cardíacos são muito comuns e ocorrem quando uma ou mais artérias coronarianas ficam bloqueadas, interrompendo o fluxo sanguíneo. O que pode provocar um bloqueio em uma artéria coronariana?
Muitos ataques cardíacos são provocados por doença dessa artéria. A aterosclerose é um tipo de doença da artéria coronariana que ocasiona depósitos gordurosos nas artérias e forma estruturas chamadas placas. Com o tempo, essas placas endurecem e estreitam as artérias, obstruindo o fluxo de sangue rico em oxigênio. As placas se tornam particularmente perigosas quando se deslocam e obstruem a circulação. Às vezes, placas soltas podem interromper por completo a circulação sanguínea, privando as células cardíacas de oxigênio e nutrientes. Imagine esse bloqueio como um enorme congestionamento de trânsito. Sem um suprimento fresco de oxigênio ou nutrientes, as células musculares do coração ficam danificadas ou morrem. A consequência é um ataque cardíaco.
Por que um ataque cardíaco é tão perigoso? Em primeiro lugar, quando as células do coração ficam famintas por nutrientes ou oxigênio, não funcionam mais. Já não dispõem do material necessário aos batimentos. Em consequência, o músculo cardíaco deixa de se contrair e o suprimento de sangue para o resto do corpo é interrompido. Mesmo que um médico elimine o bloqueio e restaure o fluxo sanguíneo após um ataque cardíaco, caso o fluxo tenha sido interrompido por algumas horas, os cardiomiócitos danificados jamais se recuperarão. Um ataque cardíaco pode provocar a perda de até um bilhão de cardiomiócitos [3]. Os cardiomiócitos danificados são substituídos por tecido cicatricial, que não ajuda o coração a bombear sangue e pode causar batimentos cardíacos anormais, enfraquecendo gravemente o coração e levando à morte súbita.
Células-tronco podem se transformar em células do coração
Você já se perguntou de onde vêm os cardiomiócitos e outros tipos de células de seu corpo? Todas as células de seu corpo começam como células-tronco (Figura 2). As células-tronco se desenvolvem em inúmeros tipos de células diferentes: da pele, dos nervos, do coração, etc. Elas se dividem com muita rapidez quando ainda não se especializaram nem assumiram tarefas específicas no corpo. Assim como as crianças crescem e escolhem uma profissão, as células-tronco amadurecem e se tornam células especializadas do corpo. Originam-se de duas fontes principais: tecidos adultos e embriões. No entanto, apenas as células-tronco embrionárias podem se tornar células-tipo no corpo.
Os cientistas aperfeiçoaram métodos para reprogramar geneticamente células adultas, transformando-as nas chamadas células-tronco pluripotentes induzidas. Tanto as células-tronco embrionárias quanto as induzidas são pluripotentes, isto é, possuem uma capacidade ilimitada de se dividir e diferenciar (transformar) em qualquer tipo de célula do corpo.
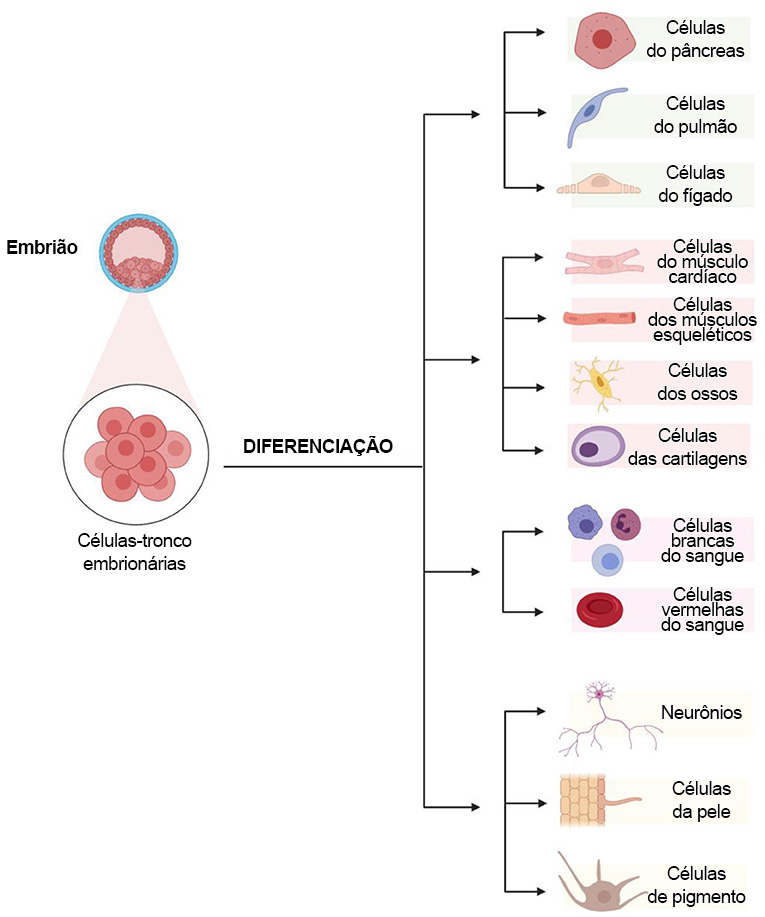
Figura 2. As células-tronco embrionárias podem se dividir rapidamente e transformar-se em qualquer tipo de célula do corpo.
A fim de produzir cardiomiócitos a partir de células-tronco em laboratório, os cientistas expõem células-tronco às mesmas moléculas de sinalização que geram os cardiomiócitos no embrião em desenvolvimento. Depois de alguns dias, os cardiomiócitos em desenvolvimento pulsam, como se pode ver ao microscópio (Vídeo 1). Os cardiomiócitos derivados de células-tronco continuam a crescer e se diferenciar por várias semanas. O resultado é um suprimento quase infinito de células funcionais dos músculos do coração, encarregadas dos batimentos. Diversos testes moleculares foram realizados para verificar a identidade e a pureza de cardiomiócitos desenvolvidos em laboratório.
Socorro, células-tronco!
A fim de ajudar os pacientes a se recuperarem após ataques cardíacos, os cientistas estão usando cardiomiócitos derivados de células-tronco para substituir o músculo cardíaco em áreas onde ele se transformou em tecido cicatricial. Um dos métodos é o chamado remendo cardíaco, um pedaço de tecido cardíaco desenvolvido em laboratório que pode ser implantado no coração para substituir o tecido danificado do paciente (Figura 3) [4].
Um remendo cardíaco é uma espécie de band-aid para um coração que sofreu lesões. Para criá-lo, células são desenvolvidas num molde (suporte) para a formação de tecido, em condições que simulam as encontradas no corpo [5]. São replicados, por exemplo, a temperatura, o oxigênio e o dióxido de carbono que existem no corpo. Uma combinação de células cardíacas é colocada no suporte, juntamente com cardiomiócitos derivados de células-tronco. Finalmente, o remendo cardíaco é implantado no coração, na esperança de que substitua o tecido cicatricial morto (e portanto incapaz de promover batimentos) por músculo funcional, capaz de promovê-los.
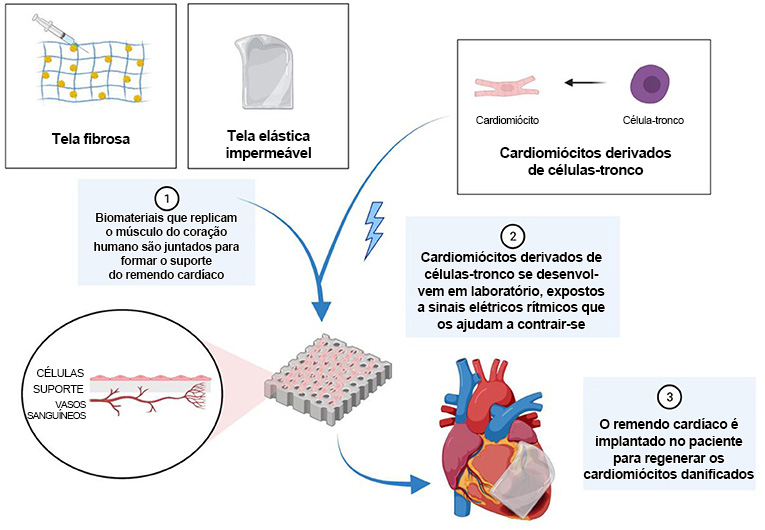
Figura 3. A fim de produzir remendos cardíacos, é preciso primeiro elaborar um suporte. Este é feito de materiais que replicam o músculo do coração humano. Em seguida, os cardiomiócitos que se diferenciaram das células-tronco são colocados no suporte. Por fim, o suporte completo é implantado no paciente para ajudar na recuperação do músculo cardíaco danificado.
Os cientistas têm pesquisado vários métodos para a implantação de remendos cardíacos. Descobriram que expor os cardiomiócitos derivados de células-tronco a sinais elétricos (“eletrocutando-os” levemente antes da implantação) melhora sua capacidade de contrair-se. Entretanto, há ainda muitos obstáculos ao uso de remendos cardíacos em terapia. Primeiro, quando um remendo cardíaco é implantado, apenas de 0,1 a 10% das células implantadas sobrevivem para se tornar cardiomiócitos funcionais [3], um número muito baixo para restaurar plenamente a função cardíaca. Também é possível que algumas das células implantadas não consigam bater ao mesmo tempo ou fazer o mesmo trabalho que o resto do coração, comprometendo o ritmo e a eficiência dos batimentos [6].
Novas descobertas são feitas constantemente no campo da regeneração do tecido cardíaco. Embora os ataques cardíacos sejam perigosos e mortais, nós, cientistas, podemos “atacá-los” usando terapias como o remendo cardíaco. Graças à ciência, conseguimos restaurar o tecido e os batimentos cardíacos, devolvendo a esperança a pacientes com corações lesionados.
As células-tronco num contexto mais amplo
As possibilidades das terapias com células-tronco são ilimitadas, ultrapassando o objetivo da regeneração cardíaca. As células-tronco podem, por exemplo, substituir células cerebrais danificadas em virtude de lesões na medula espinal ou de doenças como Alzheimer ou Parkinson [7]. Outra aplicação potencial é na produção de insulina, um hormônio que o corpo fabrica para regular os níveis de açúcar no sangue. Isso pode ajudar no tratamento de pacientes diabéticos [8]. Os cientistas não se contentam com explorar e inventar, em laboratório, maneiras de empregar as células-tronco na cura de problemas médicos: procuram também meios de usá-las para melhorar a saúde de pacientes com múltiplas doenças ou distúrbios.
Glossário
Nódulo sinoatrial (NS): ↑ Estrutura especializada do coração que aciona os batimentos cardíacos induzindo o músculo do coração a se contrair.
Cardiomiócitos: Células do músculo cardíaco que se contraem para bombear o sangue pelo corpo.
Aterosclerose: Doença provocada pelo espessamento, endurecimento e estreitamento das artérias, em resultado do depósito de placas, gorduras, colesterol e outras substâncias nas paredes internas das artérias.
Placas: Depósitos nas artérias compostos de gorduras, colesterol e outras substâncias contidas no sangue que se formam e endurecem com o tempo, estreitando as artérias e bloqueando o fluxo sanguíneo.
Células-tronco: Células-mestre que se dividem rapidamente e podem se transformar em qualquer outro tipo de célula. Células-tronco embrionárias provêm de embriões; células-tronco pluripotentes induzidas provêm de tecidos adultos que foram geneticamente reprogramados.
Pluripotentes: Células que podem se transformar em qualquer outro tipo de célula.
Remendo cardíaco: Pedaço de tecido do músculo cardíaco composto de cardiomiócitos e outros tipos de células cardíacas, desenvolvido em um suporte em laboratório e usado para reparar danos no coração.
Suporte: Estrutura feita de materiais especiais que forma uma superfície para o desenvolvimento de células, a fim de criar e moldar um pedaço de tecido.
Agradecimentos
Os autores agradecem o apoio das agências canadenses de financiamento NSERC, CIHR, NFRF e Heart and Stroke Foundation Canada. Agradecimentos também ao Ministry of Economic Development, Job Creation and Trade for an Early Researcher Award e University of Ottawa Heart Institute. Um agradecimento especial ao dr. Wenbin Liang, do University of Ottawa Heart Institute, pela disponibilização das células iPSC mostradas no vídeo.
Referências
[1] Ceconi, C., Guardigli, G., Rizzo, P., Francolini, G. e Ferrari, R. 2011. “The heart rate story.” Eur. Hear. J. Suppl. 13:C4–13. DOI: 10.1093/eurheartj/sur014.
[2] Tirziu, D., Giordano, F. J. e Simons, M. 2010. “Cell communications in the heart.” Circulation 122:928. DOI: 10.1161/CIRCULATIONAHA.108.847731.
[3] Nguyen, P. K., Rhee, J.-W. e Wu, J. C. 2016. “Adult stem cell therapy and heart failure, 2000 to 2016: a systematic review.” JAMA Cardiol. 1:831–41. DOI: 10.1001/jamacardio.2016.2225.
[4] Hosoyama, K., Ahumada, M., McTiernan, C. D., Davis, D. R., Variola, F., Ruel, M. et al. 2018. “Nanoengineered electroconductive collagen-based cardiac patch for infarcted myocardium repair.” ACS Appl. Mater. Interfaces 10:44668–77. DOI: 10.1021/acsami.8b18844.
[5] Sedlakova, V., Ruel, M. e Suuronen, E. J. 2019. “Therapeutic use of bioengineered materials for myocardial infarction.” Nanoeng. Mater. Biomed. Uses 161–93. DOI: 10.1007/978-3-030-31261-9_9.
[6] Jhang, J., Zhu, W., Radisic, M. e Vunjak-Novakovic, G. 2018. “Can we engineer a human cardiac patch for therapy?” Circ. Res. 123:244–65. DOI: 10.1161/CIRCRESAHA.118.311213.
[7] Lee, C., Willerth, S. M., Nygaard e H. B. 2020. “The use of patient-derived induced pluripotent stem cells for Alzheimer’s disease modeling.” Prog. Neurobiol. 192:101804. DOI: 10.1016/j.pneurobio.2020.101804.
[8] Jiang, W., Shi, Y., Zhao, D., Chen, S., Yong, J., Zhang, J. et al. 2007. “In vitro derivation of functional insulin-producing cells from human embryonic stem cells.” Cell Res. 17:333–44. DOI: 10.1038/cr.2007.28.
Citação
Spasojevic, A., Ruel, M., Suuronen, E. e Alarcon, E. (2022). “Can we heal a broken heart with cells?” Front. Young Minds. 10:746884. DOI: 10.3389/frym.2022.746884.
Este é um artigo de acesso aberto distribuído sob os termos da Creative Commons Attribution License (CC BY). O uso, distribuição ou reprodução em outros fóruns é permitido, desde que o(s) autor(es) original(is) e o(s) proprietário(s) dos direitos autorais sejam creditados e que a publicação original nesta revista seja citada, de acordo com a prática acadêmica aceita. Não é permitido nenhum uso, distribuição ou reprodução que não esteja em conformidade com estes termos.
Encontrou alguma informação errada neste texto?
Entre em contato conosco pelo e-mail:
parajovens@unesp.br